歡迎您訪問鄭州市第六人民醫院官方網站!



對臨床試驗默示許可公示項目審查執行程序
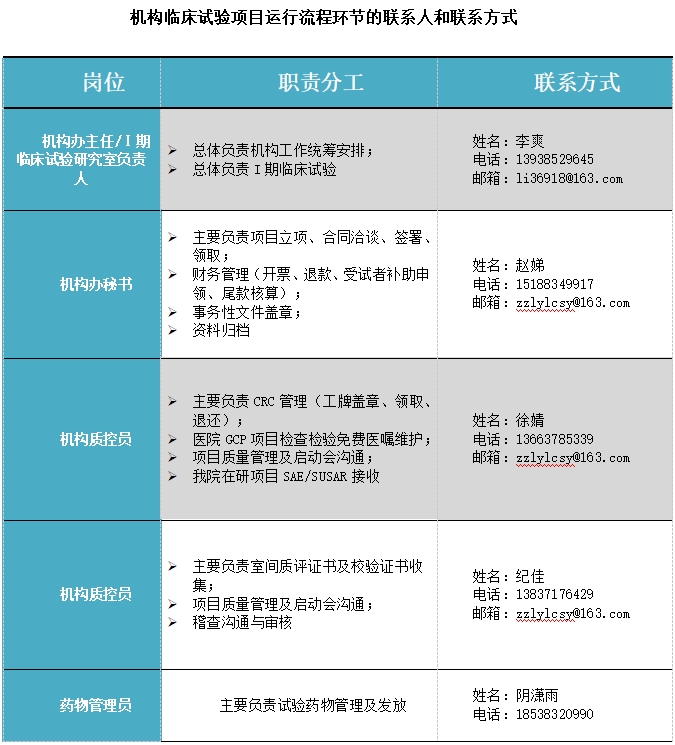
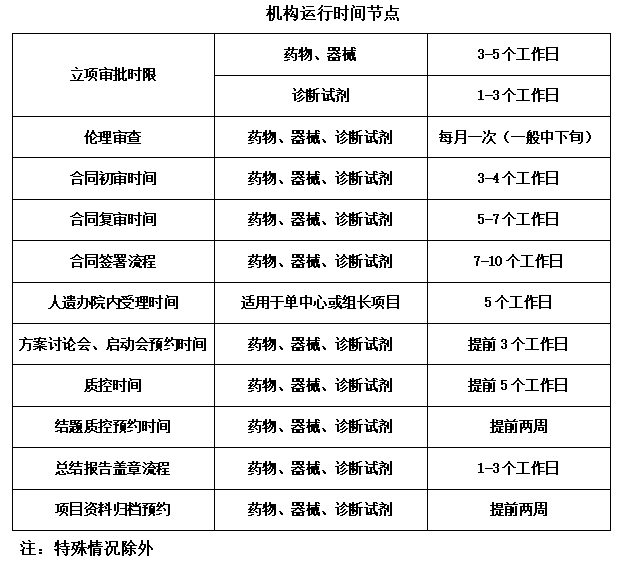
為了配合國家優化臨床試驗審批程序的要求,落實臨床試驗默示許可制的正式實施,本機構對于注冊申請人申請默許流程的臨床試驗,更新并制定相關審查執行程序。
一、臨床試驗立項審查及倫理審批階段:
無需遞交“國家藥品監督管理局藥物臨床試驗批件”。
二、臨床試驗啟動前審查階段:
需提交“臨床試驗默示許可證明材料”:
1. 國家藥品監督管理局行政許可文書受理通知書;
2. 國家藥品監督管理局臨床試驗默示許可公示截屏或通知書;
3. 開展注冊臨床試驗前與CDE溝通交流會議紀要或溝通函(加蓋申辦方公章)。
醫院地址:二七區京廣南路29號(京廣路與長江路交叉口)
乘62、81、126、203、553、556、563、906、981、B16、Y17、111、B1路直達 地鐵:五號線京廣南路站·市第六人民醫院下車向南500米
聯系電話 0371-60331627 鄭州市第六人民醫院 www.zssiyanli.com ? Copyright 2020 版權所有 豫ICP備15005665號-1
技術支持:河南維康軟件有限公司
